目前主管機關因為疫情的關係將所有級距延後至2023年底需登錄完成,真正的時間需等主管機關修法完成後公告。下表為尚未修法前的登錄期限。
|
首次取得登錄碼 日期 |
2018/12/31 以前 |
2019/01/01 以後 |
|---|---|---|
|
1~100 噸 |
2021/12/31 |
取得登錄碼以後3年 |
|
1000 噸以上 |
2020/12/31 |
取得登錄碼以後3年 |
|
關於 |
麥德凱生科股份有限公司為國內少數之生技研發服務企業,以臨床前CRO(Contract Reasearch Organization)為主軸。提供國內生技產業上、中及下游整合型之研發及行銷服務。藉由各項檢測實驗規劃及整合顧問協助國內生技廠商提升產品及技術價值,完成國內外認證及市場開拓。 |
|
臨床前試驗受託CRO
|
秉持誠實精確•專業負責的企業精神,以達到服務產業,與產業共榮的企業目標。
提供國內生技產業上、中及下游整合之研發及行銷服務為主軸。
|
999 服務客戶數 |
2884 試驗樣品數 |
2448 安全性評估 |
44 功效性評估 |
392 其他客製化評估 |
2017-2020案件統計
臨床試驗委託實際案例
醫療器材
報告通過美國FDA、歐盟CE、台灣TFDA、中國NMPA等主管機關審核。血壓脈帶、呼吸加熱器、呼吸過濾器、氣切管、呼吸麻醉面罩、針筒、骨釘、骨板、人工關節、醫美用玻尿酸、手術器械、電極貼片、腹腔穿刺套管、敷料(水膠、Chitosan)、隱形眼鏡、隱形眼鏡保養液、胃管、矯正釘、牙科矯正器(隱形牙套)、手術包、手術巾、超音波膠、抗菌濕巾、拐杖等醫療器材。
化學品
報告通過行政院環境保護署毒物及化學物質局、歐盟CE等主管機關審核。新化學品第一至第三等級登錄試驗。
農藥
報告通過農業藥物毒物試驗所審核。各式農藥原體,例如:平速爛原體、脫芬瑞原體、快克草原體、拜富寧原體、三氟敏原體等。
環境用藥
報告通過行政院環境保護署毒物及化學物質局審核。包含派卡瑞丁防蚊液等各種防蚊液。
食品
報告通過台灣TFDA審核。試驗樣品包含膠囊、錠劑、粉末、飲品…等劑型,種類包含健康食品、保健食品、機能性食品原料、食品添加物、非傳統性食品原料、植物萃取物、微生物發酵產物、動物來源食品原料、菇蕈來源食品原料、牛樟芝…等。
安全性評估試驗(體外/體內)
我們在各產業領域:醫療器材、化學品、農藥與環境用藥、健康食品/非傳統性食品原料 、藥品等,都提供了安全性評估試驗,根據國際法規OECD、ISO 10993內容,每年平均執行達800件毒理試驗,評估報告在TFDA、FDA、CE、NMPA都受到了認可。
功能性評估試驗
健康食品方面亦根據 TFDA 健康食品保健功效評估方法,建立有多種功能性評估試驗模式。
目前主管機關因為疫情的關係將所有級距延後至2023年底需登錄完成,真正的時間需等主管機關修法完成後公告。下表為尚未修法前的登錄期限。
|
首次取得登錄碼 日期 |
2018/12/31 以前 |
2019/01/01 以後 |
|---|---|---|
|
1~100 噸 |
2021/12/31 |
取得登錄碼以後3年 |
|
1000 噸以上 |
2020/12/31 |
取得登錄碼以後3年 |
在2018年前首次取得登錄碼時,以當年的噸數往前推3年,3年中最高噸數。
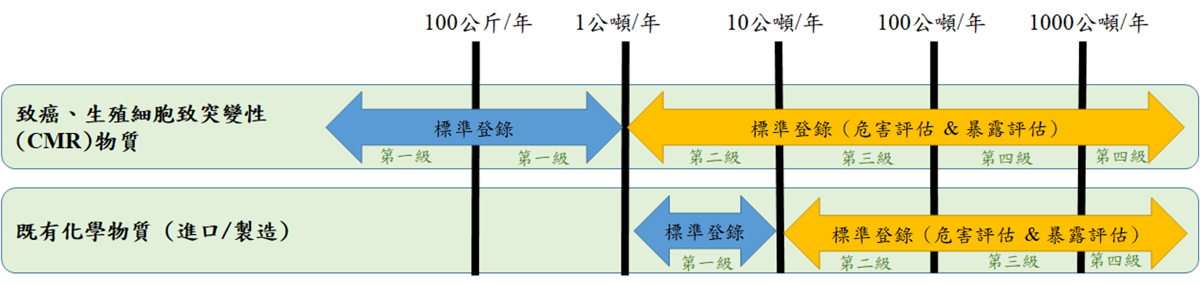
每個級距需繳交的資料不同,第一級是無需繳交危害及暴露評估,第二級到第四級的廠商,則可先提供1~7項的數據資料,在補繳危害及暴露評估資訊。
|
登錄資訊 |
第一級 |
第一級 |
第一級 |
第一級 |
|---|---|---|---|---|
| 1. 登錄人與物質辨識資訊 | V | V | V |
V |
| 2. 製造、用途與暴露資訊 | V |
V |
V |
V |
| 3. 危害分類與標示 |
V |
V |
V |
V |
| 4. 安全使用資訊 |
V |
V |
V |
V |
| 5. 物理化學特性資訊 |
V |
V |
V |
V |
| 6. 毒理資訊 |
V |
V |
V |
V |
| 7. 生態毒理資訊 |
V |
V |
V |
V |
| 8. 危害評估資訊 |
V |
V |
V |
|
| 9. 暴露評估資訊 |
V |
V |
V |
既有化學物質第一階段登錄並無效期,故不用重複登錄或展延;新化學物質則有核准登錄期限,應依登錄辦法第13條,自有效期間屆滿6個月前起算3個月之期間內提出展延申請。 而「申報」與「登錄」之作業並不相同,經核准登錄之新化學物質及既有化學物質,應依登錄辦法第24條,於核准登錄後每年4月1日至9月30日,申報前一年製造及輸入之數量資訊。
目前已公告106項化學物質為既有化學物質,如附表。
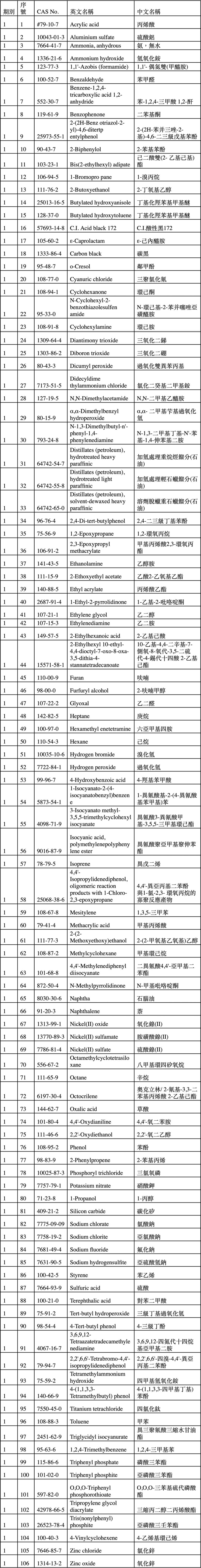
麥德凱生科為提供更完整服務,並協助客戶往國際性的發展支援,從2009年開始獲得各項專業實驗室認證,並維持這些認證直到現在。
| 認證項目 | 驗證認證 |
|---|---|
|
ISO 17025(TAF)國際品質標準認證 |
11年 |
|
OECD GLP經濟合作暨發展組織優良實驗室操作規範 |
9年 |
|
TFDA GLP藥物非臨床試驗優良操作規範認證 |
11年 |
|
ISO 9001:2000 國際品質標準認證 |
12年 |