- 法規依循
健康食品安全評估方法
OECD 471: Bacterial Reverse Mutation Test
- 試驗品系
沙門氏菌
- 試驗目的
在含有或不含有大鼠肝臟代謝酵素的情況下,評估試驗物質是否會導致微生物基因突變。
健康食品
根據健康食品管理法,為確保健康食品之人體食用安全性,健康食品需以科學化方式證明其無害人體健康,且成分具有明確保健功效。依據健康食品安全評估方法規範,產品所使用的原料不同,需進行不同類別的安全性評估試驗,主要可分為四類如下:
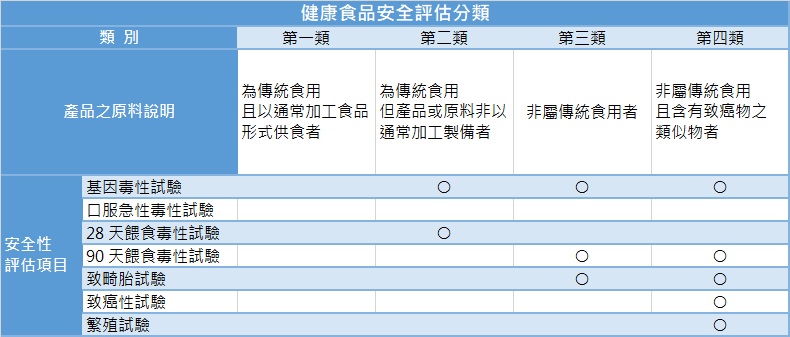
○:需進行試驗
麥德凱生科之毒理試驗具有TAF OECD GLP及TFDA GLP雙重認證,能協助依據您產品所使用的原料特性,提供完整的毒理試驗建議與服務,並可協助業者檢附相關資料,向主管機關函詢確認產品之安全性分類。如果您有需要健康食品安全性評估試驗方面的協助,歡迎聯絡我們。


- 法規依循
健康食品安全評估方法
- 試驗品系
使用哺乳類細胞株或初代哺乳類細胞
- 試驗目的
評估在含有或不含有大鼠肝臟代謝酵素 (S9 mix) 環境下,試驗物質是否會造成中國倉鼠卵巢細胞之細胞毒性與染色體結構變異。

- 法規依循
健康食品安全評估方法
OECD 474: Mammalian Erythrocyte Micronucleus Test
- 試驗品系
ICR小鼠
- 試驗目的
評估試驗物質是否會造成囓齒類動物體內周邊血液的微核發生

- 法規依循
OECD 423: Acute Oral toxicity - Acute Toxic Class Method
- 試驗品系
SD大鼠
- 試驗目的
觀察口服試驗物質後短時間內發生的不良反應,以評估試驗物質的LD50值(半數致死劑量)。

- 法規依循
健康食品安全評估方法
OECD 407: Repeated Dose 28-day Oral Toxicity Study in Rodents
- 試驗品系
SD大鼠
- 試驗目的
研究試驗物質經重複餵食28天後對哺乳類動物是否產生不良影響,並評估其無不良影響劑量(NOAEL)

- 法規依循
健康食品安全評估方法
OECD 408: Repeated Dose 90-Day Oral Toxicity Study in Rodents
- 試驗品系
SD大鼠
- 試驗目的
研究試驗物質經重複餵食90天後對哺乳類動物是否產生不良影響,並評估其無不良影響劑量(NOAEL)

- 法規依循
健康食品安全評估方法
OECD 414: Prenatal developmental toxicity study
- 試驗品系
受孕成功的雌性SD大鼠
- 試驗目的
評估試驗物質對胚胎發育之影響
