ISO 10993-1風險導向之生物評估
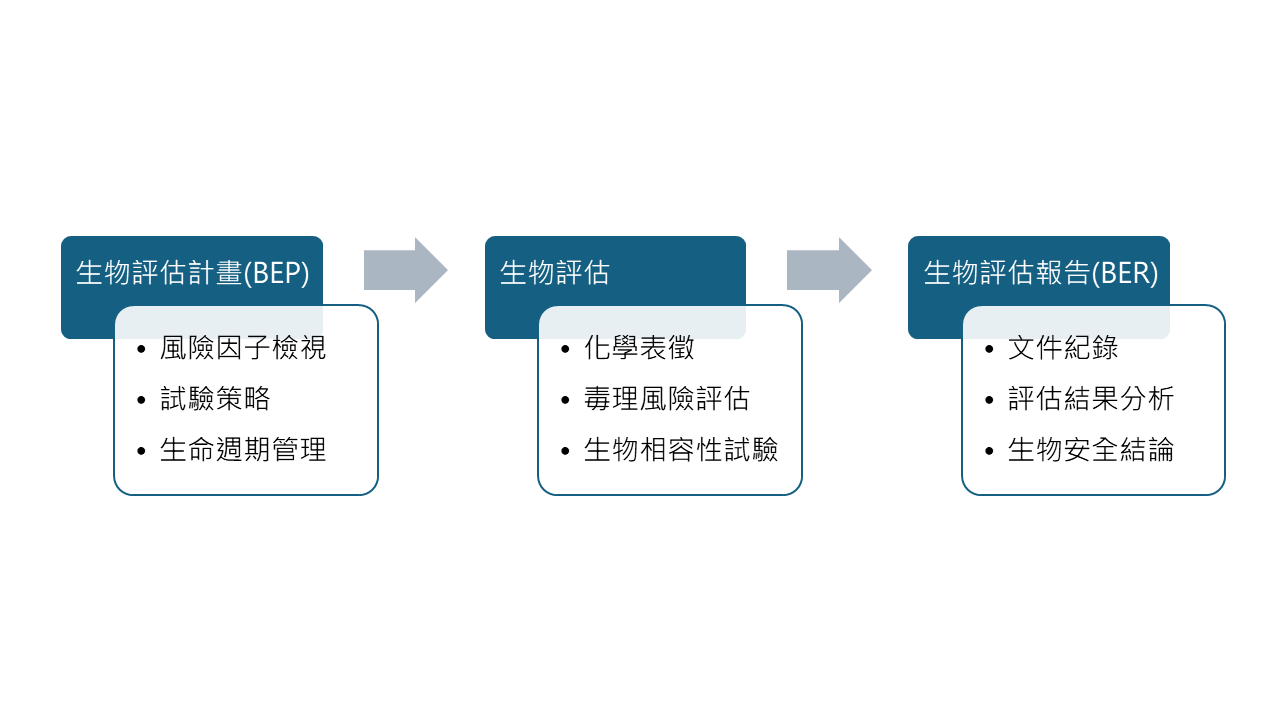
ISO 10993-1生物評估流程與ISO 14971風險管理原則深度整合,範疇涵蓋風險分析、評估、控制、剩餘風險評估及上市後監測。現行的ISO 10993-1已由單純的「試驗檢核表」轉化為系統性評估架構,旨在鑑定醫材潛在的化學、物理及生物風險。透過與類似品(Predicate Device)的差距分析(Gap Analysis)判定生物等同性(Biological Equivalence),並在產品全生命週期中落實風險控管。
制定生物評估計畫(Biological Evaluation Plan, BEP)
建立完善的BEP是符合國際法規要求並確保生物安全的起點。在研發前期即制定評估計畫,能有效精準化生物風險識別,避免不必要的重複試驗。麥德凱生科(Medgaea)結合專業團隊與科學策略,根據產品特性與現有科學文獻,為客戶制定高度法規和規性的BEP,其核心考量要素包括:
- 材料組成與物理化學特性評估
- 預期用途及合理可預見之誤用
- 人體接觸型態(部位)與暴露時間
- 潛在危害鑑定與生物風險評估
- 類似品之差距分析與數據引用
- 界定必要的生物相容性試驗範疇
撰寫生物評估報告(Biological Evaluation Report, BER)
生物評估報告(BER)是落實生物評估計畫(BEP)的關鍵產出,旨在系統性地彙整科學數據與論證結論,以證明醫療器材的生物安全性。作為產品全生命週期風險管理的核心文件,BER具備動態修訂之特性,可隨產品設計變更或上市後臨床數據進行更新。麥德凱生科協助客戶編製符合ISO 10993-1標準之專業BER,確保報告內容之科學邏輯與技術文件(Technical Documentation)高度一致,其核心架構涵蓋:
- 精確的醫材資訊描述:確保與產品規格、材料及製程描述一致
- 生物相容性試驗結果之深度分析:針對試驗數據進行合規性解讀
- 化學表徵與毒理風險評估(TRA)之統整
- 風險評估論證(Risk Assessment Justification):針對免除試驗或引用數據之合理性說明
- 整體生物安全性綜合結論
麥德凱生科提供科學嚴謹、法規導向的生物評估服務,協助客戶建構完整的安全性論述與佐證文件,以符合各國法規之嚴苛審查要求,加速產品在全球醫材市場的取證與上市進度。