- 依循標準
ISO 10993-23
- 試驗體系
倉鼠
- 萃取溶劑
生理食鹽水(Normal Saline)、棉花籽油(Cottonseed Oil)
- 試驗目的與方法
評估醫療器材引發口腔黏膜刺激反應之潛在可能性。
測試物經過萃取後,萃取液投予至倉鼠口腔頰囊中,投予4次,每次間隔約1小時,觀察其刺激反應及病理組織切片。
- 符合規範之結果
無刺激;病理切片組織無異常。
ISO 10993生物相容性試驗
生物相容性評估是醫療器材開發過程中的核心環節,旨在確保產品在預期臨床用途下的安全性。透過嚴謹的生物風險鑑別,我們能預先評估醫材與人體組織間的交互作用,從而在產品上市前有效控管潛在的生物性危害。
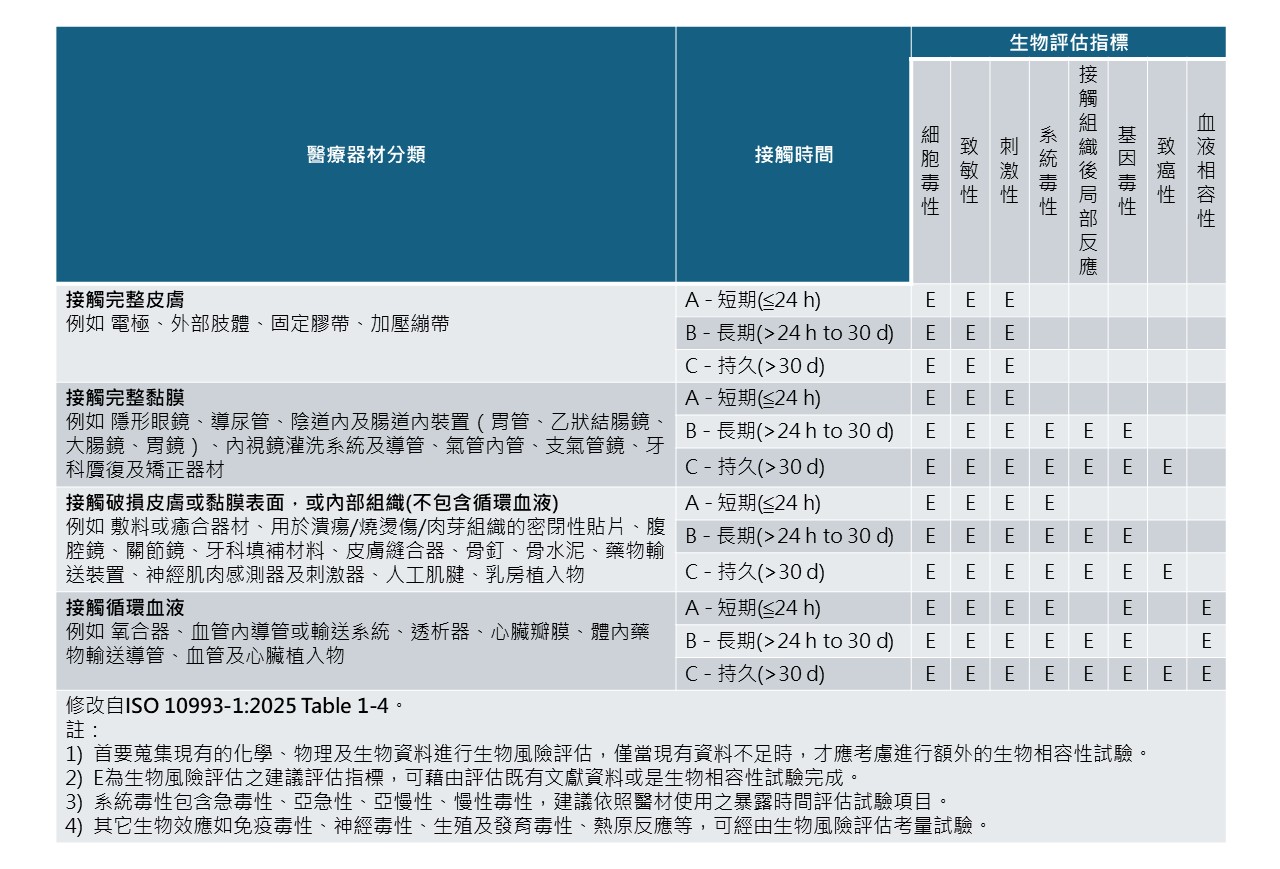
生物相容性評估的核心基礎在於細胞毒性(Cytotoxicity)、刺激性(Irritation)、敏感性(Sensitization)三項基本試驗。針對不同醫材的材質特性、預期用途、接觸型態與時間,我們將依據ISO 10993-1之風險評估架構(詳見下表),進一步評估額外的生物終點,如系統毒性、植入後局部反應、基因毒性、致癌性以及血液相容性。
麥德凱生科(Medgaea)憑藉專業技術團隊與國際級實驗室設備,致力於為客戶制定科學嚴謹且符合全球監管機構要求的生物相容性評估策略。


- 依循標準
ISO 10993-23
- 試驗體系
紐西蘭大白兔
- 萃取溶劑
生理食鹽水(Normal Saline)、棉花籽油(Cottonseed Oil)
- 試驗目的與方法
評估醫療器材引發陰道刺激反應之潛在可能性。
檢測兔子局部陰道經多次接受醫療器材類試驗物質或試驗物質萃取液後,該部位引發之刺激或炎症反應。
- 符合規範之結果
陰道無泛紅、無發腫、無異常分泌物相關臨床反應;病理切片組織無異常。

- 依循標準
ISO 10993-10
- 試驗體系
天竺鼠
- 萃取溶劑
生理食鹽水(Normal Saline)、棉花籽油(Cottonseed Oil)
- 試驗目的與方法
評估醫療器材引發接觸性過敏反應與延遲性過敏反應(delayed hypersensitivity)之潛在可能性,為最靈敏之敏感性試驗。
測試物經過萃取後,將佐劑(Adjuvant)與萃取液均勻混合,分別透過皮內注射及皮膚敷貼方式誘導,檢測是否具潛在致敏性。
- 符合規範之結果
無紅班、水腫等延遲性過敏反應。

- 依循標準
ISO 10993-4
ASTM F756
- 試驗體系
紐西蘭大白兔之血液
- 試驗目的與方法
評估接觸血液之醫療器材引發溶血現象之潛在可能性。
以直接接觸與間接接觸(萃取液)方法,將測試物的萃取液與稀釋後之兔血進行反應,檢測是否引起溶血反應。
- 符合規範之結果
與負對照組比較,溶血指數≦2%,試驗物質不會引起溶血反應。

- 依循標準
ISO 10993-11
USP 151
- 試驗體系
紐西蘭大白兔
- 萃取溶劑
無熱原生理食鹽水
- 試驗目的與方法
評估醫療器材是否存在引發熱原反應之成分。
測試物經過萃取後,將萃取液注射入耳靜脈,於3小時間,每隔半小時量測體溫變化。
- 符合規範之結果
單一大白兔體溫上升未超過0.5℃。

- 依循標準
ISO 10993-3
ISO 10993-33
- 試驗體系
沙門氏菌(Salmonella typhimurium)
- 萃取溶劑
滅菌水、DMSO、EtOH或其他溶劑
- 試驗目的與方法
評估醫療器材引發致突變性之潛在可能性
測試物經過萃取後,在含有或不含有大鼠肝臟代謝酵素(S9 mix)環境下檢測組胺酸缺陷型沙門氏菌之突變作用。
- 符合規範之結果
菌株TA97a、TA98、TA100及TA102之突變菌落數不大於負對照組2倍內,TA1533落在負對照組3倍內,則測試物不具致突變性。

- 依循標準
ISO 10993-3
ISO 10993-33
- 試驗體系
中國倉鼠卵巢細胞
- 萃取溶劑
不含血清之細胞培養液(Culture medium without serum)、含血清之細胞培養液(Culture medium with serum)
- 試驗目的與方法
評估醫療器材引發致突變性之潛在可能性。
測試物經過萃取後,在含有或不含有大鼠肝臟代謝酵素(S9 mix)環境下檢測中國倉鼠卵巢細胞之細胞毒性及染色體結構變異(包含chromosome gap、break、deletion、exchange、polyploidy and pulverization)。
- 符合規範之結果
試驗組和負對照組之染色體結構變異率無顯著差異,則測試物不具致突變性。。

- 依循標準
ISO 10993-3
ISO 10993-33
- 試驗體系
ICR小鼠
- 萃取溶劑
生理食鹽水(Normal Saline)、棉花籽油(Cottonseed Oil)
- 試驗目的與方法
評估醫療器材引發致突變性之潛在可能性。
測試物經過萃取後,以腹腔注射至試驗動物體內,分別在第48及70小時採血,並製作血液抹片,經染色後,檢測囓齒類動物體內週邊血液微核之發生率。
- 符合規範之結果
不會造成小鼠週邊血液微核發生率增加或減少,則測試物不具致突變性。

- 依循標準
ISO 10993-11
- 試驗體系
小鼠
- 萃取溶劑
生理食鹽水(Normal Saline)、棉花籽油(Cottonseed Oil)
- 試驗目的與方法
評估醫療器材引發全身急毒性反應之潛在可能性。
測試物經過萃取後,以尾靜脈注射或腹腔注射單一劑量,於投予後連續觀察3天試驗動物之臨床症狀並於期末執行剖檢觀察臟器病變。
- 符合規範之結果
無測試物引起之異常臨床症狀與全身急毒性反應。

- 依循標準
ISO 10993-11
- 試驗體系
大鼠
- 試驗目的與方法
評估醫療器材、物質成分內有否存在毒性成分。
測試物經過萃取後,於試驗期間,經由尾靜脈、腹腔投予萃取液,期間觀察動物之臨床生理之變化、體重、攝食狀況,並於期末進行剖檢,並取出體內臟器及收集血液、尿液,觀察組織病理切片及血清生化分析、尿液分析。

- 依循標準
ISO 10993-6
- 試驗體系
大鼠、大白兔
- 試驗目的與方法
評估醫療器材引發局部反應(local effects)之潛在可能性。
依據測試物之臨床適應症選擇植入部位(肌肉、骨頭、皮下、腦或其他部位),觀察其臨床症狀與分析植入物周邊組織病理反應。
